Votre Référence pour l’Hépatite C au Québec
Dépistage et diagnostic
Aux États-Unis, jusqu’en 2012 les recommandations de dépistage pour le VHC étaient basées sur les facteurs de risque. À partir de 2012, une recommandation a été introduite préconisant que tous·tes les patient·es né·es entre 1945 et 1975 devraient être dépisté·es une fois dans leur vie, indépendamment des facteurs de risque.
En 2020, le Center for Disease Control (CDC) a mis à jour ses recommandations de dépistage pour le VHC afin d’inclure le dépistage de tous·tes au moins une fois dans la vie et le dépistage des personnes enceintes à chaque grossesse.1 Cette décision fait suite aux données récentes de ce territoire qui incluent une hausse du nombre de nouveaux cas d’hépatite C, touchant particulièrement les jeunes.
Au Canada, les recommandations du Groupe d’Étude Canadien sur les Soins de Santé Préventifs se basent uniquement sur les facteurs de risque. Elles n’incluent pas le dépistage des personnes nées entre 1945 et 1975 contrairement aux demandes de l’Association Canadienne pour l’étude du foie (CASL) et du Réseau Canadien sur l’Hépatite C (CanHepC) qui plaident pour.
En 2021, la Colombie-Britannique a émis des recommandations provinciales visant à tester une fois dans leur vie les personnes nées entre 1945 et 1975.
Au Québec, le dépistage de l’hépatite C n’est recommandé que pour les personnes ayant des facteurs de risque au VHC :
- Avoir consommé des drogues par injection, même une seule fois;
- Être originaire d’un pays où le VHC est endémique (Pakistan, Egypte, Syrie, Roumanie, Europe de l’Est, Asie centrale, partie centrale de l’Afrique subsaharienne, Taiwan). À noter que le dépistage du VHC ne fait pas partie du bilan de santé requis par Immigration Canada;
- Être un HARSAH vivant avec le VIH ou qui envisage de prendre la PrEP;
- Être une personne vivant avec le VIH, atteinte d’une lymphogranulomatose vénérienne ou ayant possiblement contracté le virus de l’hépatite B par voie sanguine;
- Avoir été exposé·e à du sang ou à d’autres liquides biologiques potentiellement infectés (tatouage ou perçage dans des conditions non stériles, exposition en milieu de travail ou exposition dans un contexte non professionnel);
- Avoir subi des procédures (chirurgicales ou autres) avec du matériel potentiellement contaminé dans une région du monde où la prévalence de l’hépatite C est élevée (> 2 %);
- Avoir reçu une transfusion de sang ou de produits sanguins, une greffe de cellules, de tissus ou d’organe (au Canada, avant avril 1992);
- Être une personne enceinte chez laquelle on note des facteurs de risque associés à l’hépatite C avant ou pendant la grossesse;
- Avoir une expérience d’incarcération;
- Recevoir des services dans un centre de ressources en dépendance à des drogues;
- Être sous hémodialyse;
- Nourrissons et enfants né·es d’un parent porteur du VHC (ARN du VHC positif). Concerne uniquement le parent qui porte la grossesse.
À la liste de facteurs de risque, les recommandations de gouvernement ajoutent les conditions cliniques suivantes :
- Présenter une élévation inexpliquée de l’aspartate aminotransférase (AST) ou de l’alanine aminotransférase (ALT), ou de ces deux transaminases;
- Avoir une maladie hépatique avancée qui peut être révélée par des signes cliniques, biologiques et/ou radiologiques;
- Présenter des manifestations extra- hépatiques (MEH) évocatrices du VHC.
De plus, en théorie, toute personne qui demande un dépistage, même en l’absence de facteur de risque exprimé, devrait y avoir accès mais la mise en application de cette recommandation est inégalitaire. Or, on sait que la déclaration facteurs de risque est sous- optimale car il y a de nombreux obstacles à leur dévoilement, notamment la discrimination et stigmatisation qui peuvent y être associées. Le dépistage des personnes enceintes n’est pas encore recommandé au Québec. Nous restons à l’affût des prochaines recommandations de la Société des obstétriciens et gynécologues du Canada (SOGC). Nous notons cependant que c’est une pratique en hausse.
Le dépistage d’une hépatite C chronique est effectué le plus souvent à partir d’une prise de sang et se déroule en deux étapes :
- Tout d’abord un dépistage des anticorps anti-VHC visant à savoir si la personne a été exposée au VHC;
- Puis, un test ARN VHC visant à déterminer si la personne est porteuse d’une hépatite C active (ou virémique).
Suite à exposition au VHC, une personne développe des anticorps en 6 à 8 semaines. La période fenêtre pour le dépistage du VHC est de 12 semaines. Il est important de noter que cette durée peut être allongée en cas de co- infection VIH-VHB.
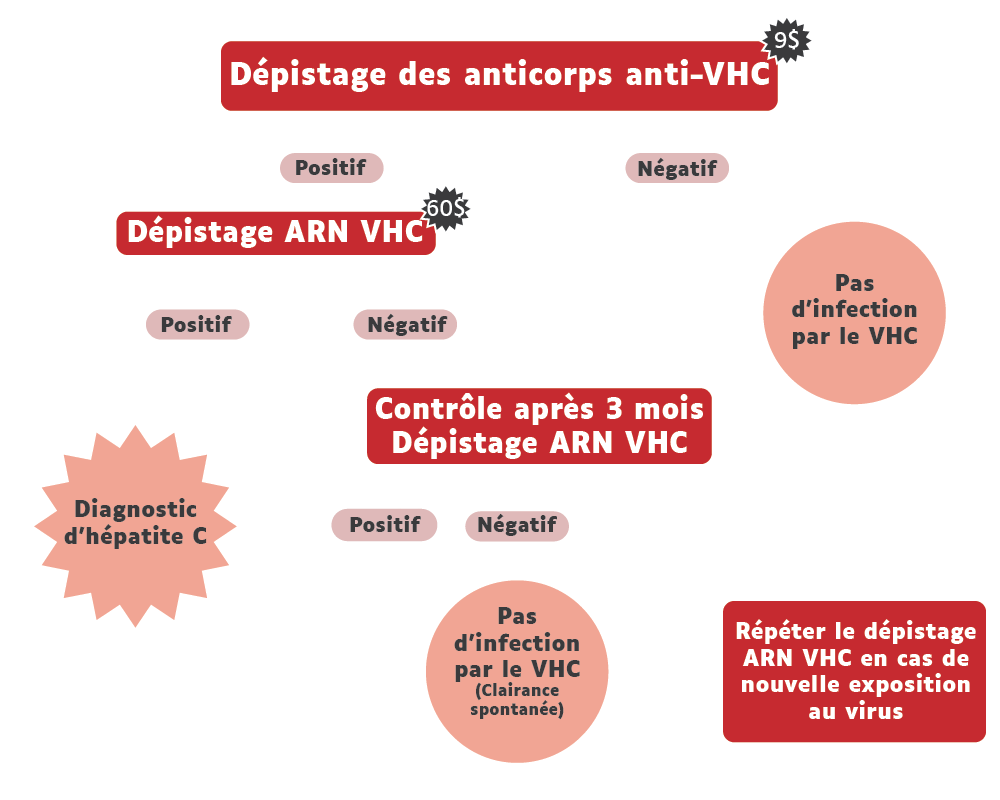
Les anticorps anti-VHC sont présents chez toutes les personnes qui ont été en lien avec le virus, mais contrairement aux anticorps anti-VHB, ils ne sont pas protecteurs. Une personne qui n’a jamais fait de sérologie anti-VHC se verra prescrire un test anticorps anti-VHC. Ce test est réalisé en première intention car son coût est beaucoup moins élevé que celui du test ARN (9$ versus 60$).
- Si le test anticorps est négatif, c’est la fin des investigations, la personne n’a pas été exposée au VHC.
- Si le test anticorps est positif, la personne a été exposée au VHC. Il faut désormais déterminer si elle fait partie des 15 % à 40 % de personnes qui se débarrassent spontanément du virus ou si elle est porteuse du virus.
Suite à un test anticorps anti-VHC positif, on procède donc à un test ARN-VHC qui va indiquer la charge virale, soit la mesure de la quantité de virus par ml de sang. Ce test indique désormais à la fois l’ARN qualitatif et la charge virale quantitative. L’ARN-VHC est présent dans le corps dès l’exposition au virus.
- Si le test est positif: la personne est virémique, elle est porteuse d’une hépatite C chronique.
- Si le test est négatif: cela suggère que la personne fait une clairance spontanée du virus. Cependant, un contrôle aux 3mois est recommandé pour confirmer ce résultat.
Si la personne a déjà obtenu un résultat de dépistage anticorps anti-VHC positif (par exemple pour une personne ayant reçu un traitement et guérie du VHC) alors il est recommandé de procéder directement au test ARN-VHC. Si l’exposition au VHC est confirmée, par exemple suite à une piqûre avec une seringue utilisée par une PVVHC, il est possible d’effectuer un test ARN à 4 semaines.
L’hépatite C fait partie des maladies à déclarations obligatoires (MADO) cela signifie que le médecin doit déclarer chaque nouveau cas à la direction de santé publique du lieu de résidence de la personne visée par cette déclaration.
Le génotypage n’est plus nécessaire avant le lancement du traitement grâce aux traitements pangénotypiques. Cependant, il est possible que les professionnel·les de santé demandent un génotypage (sans pour autant repousser le début du traitement) pour les personnes plus à risque de re-contracter le VHC, afin de pouvoir dissocier un échec au traitement d’une réinfection dans le futur.
Le dépistage du VHC est fréquemment réalisé via une prise de sang. Cependant, il existe d’autres méthodes et technologies.
Tests rapides
Les tests rapides permettent de procéder au dépistage des anticorps anti-VHC à partir d’une ponction capillaire ou d’un échantillon de salive. Les résultats sont disponibles en 1 minute (INSTI® HCV Test) à 20-40 minutes (OraQuick® HCV Rapid Antibody Test) selon les modèles de tests. Pour le moment, seul l’OraQuick® est homologué au Canada et uniquement utilisé à partir d’une ponction capillaire.
Dans ce contexte d’utilisation, sa sensibilité (la probabilité du résultat positif du test chez les sujets porteurs de la maladie) est de 95,9 % et sa spécificité (la probabilité du résultat négatif de test chez les patient·es défini·es comme non malades) est de 99 %. Selon une étude récente, le temps d’attente pour la lecture des résultats peut même être réduit à 5 minutes sans perdre en qualité pour identifier les patients virémiques.
Ces tests rapides sont notamment utilisés pour proposer du dépistage aux points de services : dans les organismes communautaires, les pharmacies, dans la rue… Ils permettent ainsi un accès facilité : pas de prise de rendez-vous nécessaire, réduction du temps d’attente des résultats et donc du stress associé, possibilité d’offrir de meilleures conditions de dépistage dans un environnement familier et non médical…

Ces tests ne permettent pas d’obtenir un diagnostic d’hépatite C. En cas de résultat positif, il faut orienter les personnes vers un corridor de soins afin qu’elles puissent avoir accès à un test ARN-VHC.
Au Québec, selon la Loi sur la Santé et les Services Sociaux, le dépistage est un acte réservé aux médecins, infirmier·ières et sage-femmes. Dans d’autres pays, tels que le Royaume-Uni, l’Australie ou encore la France, ces tests peuvent être proposés par des travailleur·euses communautaires ou des pairs formé·es. Compte-tenu du contexte actuel de pénurie d’infirmier·ères et de la difficulté d’accès au dépistage, empirées par la pandémie de COVID-19, il serait important de rendre cet acte accessible à d’autres professions. Les travailleur·euses communautaires qui œuvrent en lutte contre le VIH et les ITSS ont une place privilégiée pour rejoindre les communautés les plus touchées et sont des partenaires indispensables si nous souhaitons atteindre les objectifs d’élimination de l’hépatite C. De plus, la décentralisation des soins est un élément essentiel de la stratégie de l’OMS contre les hépatites.
C’est pourquoi le Comité Provincial Hépatite C, coordonné par le CAPAHC, est engagé dans un travail de plaidoyer pour obtenir une autorisation gouvernementale.
Si des autotests sont disponibles au Canada pour le VIH depuis novembre 2020, ce n’est pas encore le cas pour le VHC. Pour cela, il faudrait qu’un fabricant dépose une demande d’homologation de sa technologie pour un usage sous forme d’autotest à Santé Canada.
Tests REFLEX
Ce processus permet de réaliser le test ARN (en cas de test anticorps anti- VHC positif) à partir du même échantillon sanguin qui a servi à faire le test anticorps, il requiert uniquement de prélever un tube supplémentaire lors de la prise de sang. Les tests Reflex peuvent également être pratiqués à partir des gouttes de sang séché (voir après). Il permet donc de réduire le nombre d’étapes du diagnostic, en réduisant le nombre de consultations et de prélèvements. Cette méthode est déjà implémentée dans huit provinces canadiennes dont l’Alberta, la Colombie-Britannique et le Nouveau- Brunswick, mais pas au Québec.
Gouttes de sang séché
Ce test consiste à colliger des gouttes de sang venant d’une ponction capillaire sur un papier filtre afin de pouvoir les analyser à posteriori. Cela permet de proposer du dépistage dans des zones où moins de matériel est disponible. Les papiers filtres peuvent également être envoyés au laboratoire par voie postale. Ce dispositif permet de réaliser à la fois les tests anticorps anti-VHC pour lesquels il a une sensibilité de 98 % et une spécificité de 99 % et l’ARN-VHC pour lequel il a une sensibilité de 98 % et une spécificité de 98 %.
GeneXpert®
Cette machine permet de réaliser des tests PCR en 60 à 100 minutes. Elle permet de réaliser de nombreux tests, incluant le SARS- CoV2, le VPH, le VIH et le VHC. Elles ne sont pas encore homologuées par Santé Canada pour les tests VHC. Action Hépatites Canada a demandé au fabricant CepHeid de prioriser la demande d’homologation pour les tests VHC.
Il existe une multitude d’options de dépistage du VHC, toutes ne sont pas encore disponibles au Québec et nous savons qu’en accroissant le nombre d’options disponibles nous augmenteront le nombre de personnes rejointes. Il est important de souligner que la pandémie de COVID a impacté l’accès au dépistage. Un étude a démontré qu’en Ontario le dépistage du VHC n’est pas revenu au niveau pré-pandémie.
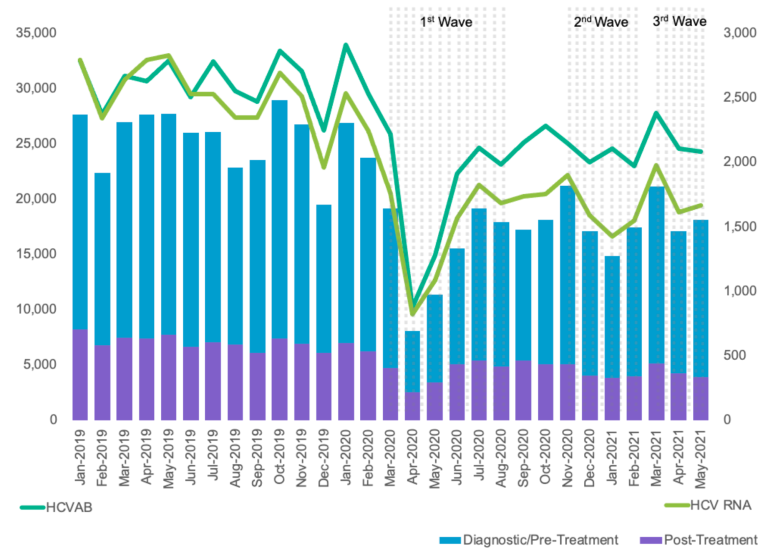
Impact de la pandémie de COVID-19 sur le
dépistage de l’hépatite C en Ontario, Canada






